- English
- Francais
You are here
GRN1005 : un nouveau médicament ciblé prometteur dérivé des taxanes
Dérivé ciblé innovant des taxanes, GRN1005 (anciennement ANG1005) représente le premier produit oncologique exploitant la voie du récepteur LRP-1 pour traverser la barrière hématoencéphalique (BHE) et pénétrer dans les cellules cancéreuses.
Des données cliniques solides de phase I démontrent que GRN1005 est hautement actif en chimiothérapie à agent unique, et son action sur le SNC dans les cancers du cerveau en fait désormais un bon candidat pour les études de phase II.
La petite molécule a donc été cédée sous licence à Geron Corporation pour un développement plus poussé.
Mécanisme d’action de GRN1005
- GRN1005 pénètre dans le cerveau en ciblant la protéine liée au LRP-1 (low-density lipoprotein receptor-related protein) qui est l’un des récepteurs les plus exprimés à la surface de la BHE.
- À l’intérieur du cerveau, GRN1005 pénètre dans les cellules cancéreuses en utilisant la cascade biologique facilitée par ce même récepteur LRP-1 qui est régulée à la hausse dans diverses tumeurs cancéreuses, notamment le gliome malin et les cancers métastasés au cerveau.
Données cliniques relatives à GRN1005
GRN1005 a été évalué dans le cadre de deux essais cliniques de phase I multicentriques distincts, menés en ouvert, à doses croissantes, visant à établir la dose maximale tolérée (DMT) et à obtenir des données préliminaires sur l’innocuité, le profil de tolérance et l’efficacité chez des patients déjà traités pour des tumeurs solides avancées avec métastases au cerveau, de même que chez des patients atteints de gliome malin récurrent.
Évaluation de GRN1005 dans les métastases cérébrales progressives
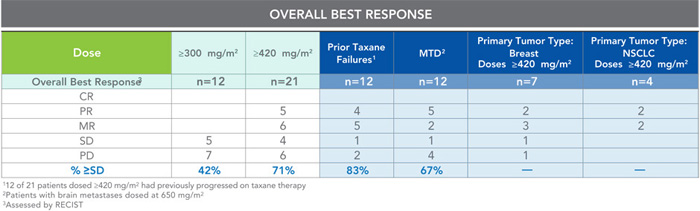
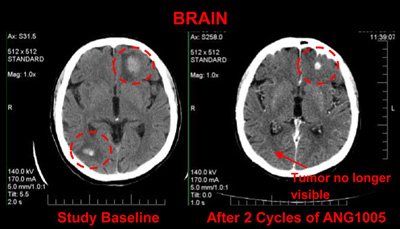
Principaux résultats : GRN1005 a présenté des indications préliminaires d’activité comme agent unique sur des métastases cérébrales provenant d’un éventail de tumeurs épithéliales malignes, dont le carcinome pulmonaire non à petites cellules (NSCLC), le cancer du sein et le cancer de l’ovaire.
Au cours de l’essai clinique de phase I, le taux de réponse des patients ayant reçu des doses thérapeutiques de GRN1005 a été de 24 % (5/21). À la DMT, le taux de réponse a été de 42 % (5/12).
En outre, 33 % (4/12) des patients précédemment traités par un taxane ont répondu au traitement par GRN1005, ce qui signifie que ce dernier est potentiellement efficace contre les tumeurs résistantes au paclitaxel.
Outre les métastases au cerveau, des réponses ont également été observées dans les métastases osseuses, hépatiques et lymphatiques.
Évaluation de GRN1005 dans le glioblastome récurrent
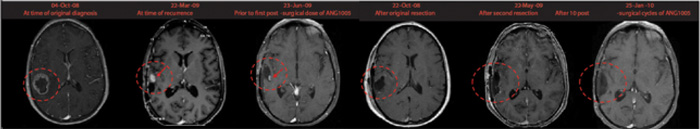
Principaux résultats : Dans l’essai clinique de phase I relatif au glioblastome récurrent, 14 % (4/28) des patients ont répondu au traitement par GRN1005, dont deux ont obtenu une réponse complète.
Des doses thérapeutiques de GRN1005 ont été retrouvées dans des échantillons de tumeur cérébrale prélevés chez des patients ayant reçu une dose unique du médicament, indiquant que celui-ci est parvenu à traverser la BHE, puis à se concentrer dans la tumeur, et ce, sans toxicité nerveuse centrale ou immunogénicité apparentes.
À la DMT, les concentrations plasmatiques de GRN1005, à savoir la concentration maximale (Cmax) et l’aire sous la courbe (ASC) ont été plusieurs fois supérieures à celles observées précédemment avec le paclitaxel nu
Les toxicités liées à GRN1005 ont été comparables à celles des autres taxanes comme le paclitaxel, avec une toxicité dose limitante due à une neutropénie.
Données présentées à l’ASCO 2010
Des données provenant des essais cliniques de phase I sur GRN1005 (anciennement ANG1005) ont été présentées à la réunion annuelle 2010 de l’American Society of Clinical Oncology (ASCO) à Chicago
> Téléchargez les affiches et les exposés
ASCO_2010_ANG1005_Malignant_Glioma.pdf
ASCO_2010_Solid_Tumours.pdf
Angiochem_LRP1_ASCO_2010_Castaigne.pdf
Angiochem_ANG1005_ASCO_2010_Drappatz.pdf
Autres études en cours de discussion
Un programme de phase II a notamment pour objectifs de confirmer l’activité clinique de GRN1005 observée au cours de l’étude de phase I dans les métastases cérébrales (provenant du NSCLC et du cancer du sein), d’identifier les sous-populations de patients appropriées dans lesquelles le taux d’activité est le plus élevé afin de réunir un maximum de patients et de prendre une décision concernant le passage à des études d’enregistrement.
